
陽イオンと陰イオン
すべての物質は原子でできています。たとえば水は水素原子2つと酸素原子1つからできています。水素原子の記号はH、酸素原子の記号はOで表わし、水はH2O(2は小さい表記)となることは多くの方がご存じですね。原子は現在100以上あって、宇宙の物質はすべて原子でできています。
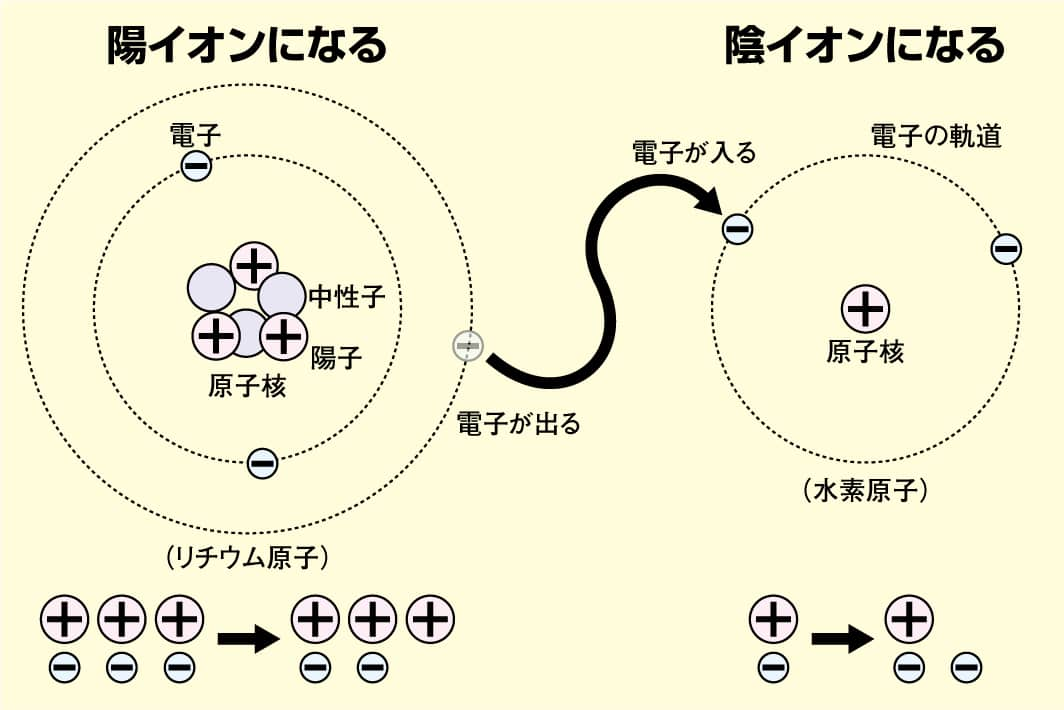
原子は中心に原子核があり、その周りを-(マイナス)電気を持った電子が回っています。そして原子核は+(プラス)の電気を帯びた陽子と電気を帯びていない中性子で構成されています。
通常、陽子と中性子、そして電子の数は同じで原子全体は+電気と-電気が打ち消し合っています。これを電気的に中性の状態といいます。ただ、電子は陽子に比べて非常に小さいため、実際には移動しやすく原子から出たり入ったりしています。この電子の出入りがあると、原子全体は電気を帯びたイオンになります。
原子から-の電子が飛び出すと全体が+の電気を帯びた陽イオンに、逆に原子に電子が取り込まれると全体が-の電気を帯び陰イオンになります。そして、イオンになる時に移動する電子を利用した道具が電池なのです。
ウキにリチウム電池が使われるわけ
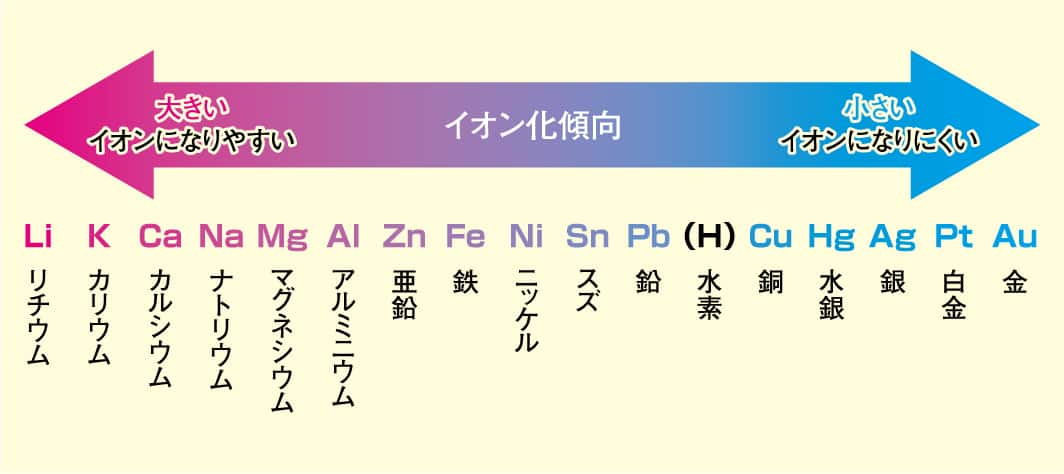


初期のボルタ電池(電池の元祖)は、亜鉛板と銅板を導線でつなぎ、電気を流すことのできる硫酸などの電解液に入れて作られていました。二つの違う金属を電解液に入れるとイオン化傾向の大きい金属は電子を出して溶けていきます。この時出た電子が電流となります。ボルタ電池の場合、銅より亜鉛の方がイオンになりやすく、電子は銅板の方に流れていき電流が発生します。しかし、電解液が液体なので持ち運びが困難でした。
その後普及することになる乾電池は、亜鉛系の物質と金属の代わりに炭素が使われ、電解液は固体の粉末になり持ち運びが可能になったものです。ただ、電極に重たい金属を使用していたので、小さな電気器具には不向きという不便さは残りました。
そこで軽い金属を使う電池の研究が進みました。その際、注目されたのがイオン化傾向の大きいリチウムでした。ただ、リチウムはすぐにイオンになる分、劣化もするので直接電極には使用できません。それを克服するため酸化物を利用しました。イオン化傾向が大きいため高い電圧を出すことができ、なおかつ軽いリチウム電池は、我々の生活に欠かせない物となっています。釣りにおいても、たとえば軽量化が必要だった電気ウキにはこのリチウム電池が最適でした。
そして現在では、リチウム電池から進化したリチウムイオン電池と言われる、充電可能な二次電池も作られています。この電池は鉛などの重い金属を利用していた今までの二次電池に比べ、かなり軽量化したため電動リールの電源などとして普及しています。また、充電可能回数も格段に増え、スマホやカメラなど小型電気器具にも使われていて、これからも普及していくと考えられます。
- 記載の内容は2021年9月現在の情報です。変更となる場合があるのでご注意ください。
- 写真はすべてイメージです。













